¿Cuántas gotas tópicas son demasiadas?

No todos los pacientes pueden lidiar con un régimen complejo, pero las opciones como las gotas combinadas están facilitando las cosas.
(Este artículo fue traducido, adaptado e impreso con autorización exclusiva del grupo de revistas de Review de Jobson Medical Information. Su reproducción está prohibida).
Dra. Janet B. Serle, MD,
Ciudad de Nueva York
Como clínicos, somos solucionadores de problemas. Hoy en día, tenemos muchas herramientas que podemos usar para administrar el glaucoma y ayudar a preservar la visión de nuestros pacientes, por lo tanto, una pregunta que nos esforzamos constantemente en responder es, ¿Cuáles son las herramientas más adecuadas para resolver el problema de este paciente? Y, ¿Cuántas de esas herramientas debemos utilizar para obtener el mejor resultado posible?
Los medicamentos tópicos siguen siendo un pilar del tratamiento del glaucoma, y hoy en día tenemos más variedades para elegir que nunca antes. Actualmente, hay siete clases de compuestos que están disponibles:
Análogos de prostaglandinas, incluida una prostaglandina que dona óxido nítrico (instilada una vez al día).
Inhibidores de la cinasa Rho (una vez al día).
Bloqueadores beta (una vez al día).
Agonistas alfa (dos o tres veces al día).
Inhibidores de la anhidrasa carbónica (dos o tres veces al día).
Mióticos (de una a cuatro veces al día).
Agonistas adrenérgicos no selectivos (dos veces al día).
Para la mayoría de los pacientes, las gotas tópicas son una forma menos arriesgada de gestionar el glaucoma que las cirugías tradicionales, tales como la trabeculectomía y el tubo de implantación de derivación. Por esa razón, la mayoría de los cirujanos estarían de acuerdo en que, si las gotas pueden controlar la enfermedad, prevenir la progresión y ser administradas de manera consistente y toleradas por el paciente, entonces esa es la opción de elección. (Las cirugías para glaucoma mínimamente invasivas (MIGS), ahora agregadas a nuestras opciones de tratamiento, deben evaluarse cuidadosamente en comparación con el tratamiento médico, en términos de eficacia y efectos secundarios, para cada paciente individual).
Esta proliferación de medicamentos para el glaucoma, particularmente con la reciente incorporación de nuevos medicamentos, la prostaglandina donadora de óxido nítrico Vyzulta, que es un co-fármaco, y el inhibidor de la Rho-cinasa, Rhopressa (así como la combinación de dosis fija de netarsudil y latanoprost, Rocklatan): ha planteado preguntas importantes ¿Cuántos medicamentos deberíamos pedir a nuestros pacientes que usen? ¿Cuántos serán bien tolerados? ¿Y cuántos van a ser efectivos?
Problemas relacionados con gotas múltiples
Pedir a los pacientes que usen gotas múltiples plantea una serie de posibles preocupaciones, que van desde qué tan bien van a funcionar las gotas cuando se agreguen a un régimen existente, hasta cómo va a afectar el manejo de las gotas múltiples el cumplimiento. Esto es lo que sabemos acerca de estos temas, a partir de la literatura publicada:
No se va a obtener tanta reducción de presión cuando se use una gota como un segundo o tercer medicamento. Cuando usamos un solo medicamento, tenemos una idea bastante acertada de cuánta presión intraocular vamos a obtener. Por ejemplo, con el uso de solo beta bloqueadores se obtendrá una reducción de la presión intraocular de un 25% a 28%. Pero si se añade un bloqueador beta al latanoprost, como segundo medicamento, el efecto será menor. En resumen, los medicamentos segundo, tercero y cuarto en el régimen de un paciente no le darán el mismo rendimiento que obtendría al usarlos en primera línea. Hemos visto esto en ensayos clínicos aleatorizados, típicamente de fase III, que generalmente comparan un medicamento con otro (a menudo timolol).1
El efecto beneficioso de un segundo, tercer o cuarto medicamento, podría no durar. Los datos de la literatura sugieren que el efecto de una medicación añadida disminuye con el tiempo.2 Sin embargo, es importante observar que esta conclusión está basada en los datos de una población de pacientes; un paciente individual puede no reflejar estos hallazgos. Por esa razón, el tratamiento de cada paciente es parte prueba y parte error. Se prescribe un medicamento para ver si funciona, y si es así, durante cuánto tiempo funciona. Cualquiera que sea el resultado, su próximo paciente podría tener una reacción diferente.
Un régimen complejo con múltiples medicamentos, puede menoscabar el cumplimiento. Para muchos pacientes va a resultar frustrante administrar múltiples medicamentos; algunos simplemente van a tener dificultad para recordar cuándo tomarlos. Otros posibles problemas incluyen el aumento del costo asociado con más medicamentos, efectos secundarios que disgustan a los pacientes y la edad del paciente. Los pacientes jóvenes que no usan muchos productos farmacéuticos pueden no tomar el régimen tan en serio como deberían. Los pacientes mayores pueden tener cambios en el estado mental o dificultad para instilar las gotas. Además, sabemos que el nivel de educación y la información sobre salud, pueden ser barreras para el cumplimiento.3
La eficacia nocturna puede ser un problema. Los estudios nocturnos que involucran medicamentos para el glaucoma, han revelado que varias clases de compuestos son menos efectivos por la noche que durante el día.4 Esa falta de eficacia en la noche puede conducir a la progresión en pacientes que parecen estar bien controlados en las mediciones de PIO durante el día. Por esa razón, cuando se trata de diseñar un régimen, hemos de asegurarnos de que se incluyen medicamentos que funcionan por la noche, así como durante el día. Además, si hay alguna duda acerca de que la progresión está ocurriendo, es importante considerar la posibilidad de que la progresión se deba a la fluctuación nocturna de la PIO. Si es así, hay que reorganizar el régimen para asegurarse de abordar la PIO nocturna.
La terapia médica crónica puede conducir a cambios conjuntivales y enfermedades de la superficie ocular. Esto sucede, en parte, como resultado de la inflamación de la conjuntiva. Sabemos que los cambios pueden estar relacionados con los conservantes, los medicamentos por sí mismos y/o la frecuencia de dosificación. Estos cambios conjuntivales pueden tener múltiples consecuencias, incluyendo visión borrosa e incomodidad para los pacientes.5 También pueden conducir a una tasa de éxito reducida en una subsecuente cirugía incisional.6 Por lo tanto, cuantas menos gotas podamos recetar sin dejar de prevenir la progresión, mejor.
A pesar de las advertencias que acabamos de mencionar, está claro que los médicos que tratan el glaucoma, usan todas las opciones de tratamiento disponibles. Podemos ver esto en la literatura. Los pacientes inscritos en el ensayo AGIS, que se realizó antes del advenimiento de las prostaglandinas, los agonistas alfa adrenérgicos y los CAI tópicos, recibieron una cantidad promedio de 2.7 medicamentos al inicio del estudio.7 A mediados de los 90, se aprobaron esas tres clases de compuestos; la cantidad de medicamentos de referencia en poblaciones de pacientes similares que participaron en ensayos clínicos posteriores fue más de tres.8,9 Los artículos actuales revisados por colegas y los informes de casos confirman un número aún mayor de medicamentos de referencia (3.6 hasta cinco).10-12 Entonces, a pesar de ser conscientes de las limitaciones de las gotas múltiples, todavía tendemos a usar una buena cantidad de medicamentos en los pacientes cuando creemos que los necesitan para reducir la PIO. (Ver tabla 1)
Eficacia al añadir un 3er o 4to medicamento para disminuir la PIO
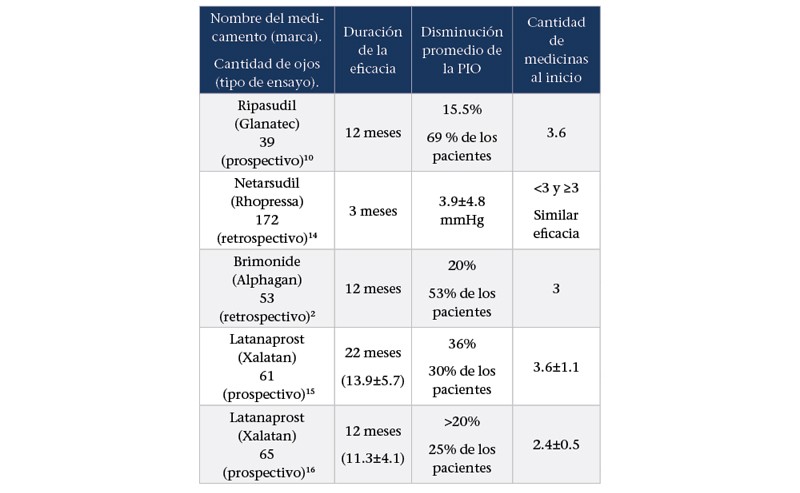
Tabla 1. Eficacia al añadir un 3er o 4to medicamento para disminuir la PIO.
Gotas tercera y cuarta
Dicho esto, ¿qué sabemos acerca de la adición de un tercer o cuarto medicamento para el régimen de un paciente? Unos cuantos estudios en la literatura han abordado esta cuestión. (Ver la tabla de arriba.) Por ejemplo:
Un estudio prospectivo de 12 meses realizado en Japón monitoreó el efecto de Ripasudil (una gota de inhibidor de la rho-cinasa administrada dos veces al día, que solo está disponible en Japón) cuando se agrega a los regímenes de pacientes con una línea base promedio de 3.6 medicamentos. Este fue el cuarto o quinto medicamento para algunos de estos pacientes, pero más de dos tercios de ellos tuvieron una reducción adicional de la PIO de casi 16%.10
Un estudio retrospectivo de 12 meses en el que se agregó brimonidina a un régimen inicial de tres medicamentos, encontró que un poco más de la mitad de los pacientes obtuvo una reducción adicional del 20% en la PIO.
Otro estudio siguió a 172 ojos durante tres meses después de que se agregó netarsudil a los regímenes de referencia. El resultado fue una reducción adicional de la presión media de aproximadamente 4 mmHg. Es de destacar que la eficacia de la adición de netarsudil fue similar, independientemente de si los pacientes estaban en menos o más de tres medicamentos al inicio del estudio.13
Varios estudios prospectivos han analizado la posibilidad de agregar latanoprost a pacientes que ya toman de 2.4 a 3.6 medicamentos.14,15 En estos estudios, se observaron reducciones adicionales de la PIO, que van desde un poco más del 20% hasta el 36%. Sin embargo, esto sólo se observó en una minoría de pacientes (de 25% a 30%). Por lo tanto, el latanoprost no proporcionó una reducción de PIO adicional tan sólida como se había anticipado.
¿Qué pasa con el uso de gotas de combinación fija como tercer y cuarto medicamento? Sabemos que los regímenes de combinación fija pueden ayudar a abordar la eficacia, la conformidad y toxicidad de la superficie. Resulta que también pueden reducir las fluctuaciones de la PIO intradiarias e interdiarias,16 lo cual puede contribuir a la progresión.17 Esto podría ser el resultado de un mejor cumplimiento, ya que se deben manejar menos gotas o el resultado de eliminar el problema de la segunda gota que lava a la primera gota si la segunda se instila demasiado rápido, después de la primera. (Esto obviamente no es una preocupación con una gota de combinación.)
Actualmente en Estados Unidos existen varias terapias de combinación de dosis fija disponibles:
- Una combinación a dosis fija de netarsudil y latanoprost (Rocklatan, aprobada en 2018).
- Una combinación de dosis fija de brinzolamida y brimonidina (Simbrinza, aprobada en 2013).
- Una combinación de dosis fija de un CAI tópico y un bloqueador beta (Cosopt, aprobada en 1998).
- Una combinación de dosis fija de brimonidina y un bloqueador beta (Combigan, aprobada en 2007).
- El co-fármaco latanoprosteno bunod, una prostaglandina que dona óxido nítrico (Vyzulta, aprobado en 2017).
Además, varios agonistas de prostaglandina / combinaciones de bloqueador beta están disponibles comercialmente fuera de los Estados Unidos (por ejemplo, Xalcom).
El desafío al que nos enfrentamos es que hay pocos, y solo retrospectivos, estudios hasta la fecha que involucren la aditividad de los nuevos medicamentos combinados a los regímenes existentes13,18 Por supuesto, sabemos bastante sobre su uso como agentes únicos de los numerosos ensayos clínicos de fase III que han sido publicados.19-21.
Contando las gotas
Una preocupación con la prescripción de múltiples gotas, es cómo evaluar la carga que un régimen determinado le impone al paciente. Propongo que en lugar de contar los medicamentos o la cantidad de frascos que usa un paciente, deberíamos contar la cantidad de instilaciones diarias de gotas para los ojos que el paciente tiene que realizar. Esto, creo, se relaciona mejor con lo que un paciente puede cumplir.
Desde esa perspectiva, las combinaciones de medicamentos y dosis fijas de hoy en día pueden permitirnos recetar más medicamentos sin aumentar el número de gotas, lo cual puede marcar una gran diferencia para muchos pacientes. Por ejemplo, si prescribimos latanoprostene bunod (Vyzulta) con netarsudil (Rhopressa) o timolol, esto significaría dos gotas al día que ofrecen tres medicamentos. Ambos Vyzulta y Rhopressa serían usados por la noche, lo cual para algunos pacientes haría que el régimen fuera más fácil de cumplir. Típicamente, timolol sería utilizado por la mañana, por lo que la combinación con Vyzulta significaría una gota en la mañana y otra por la noche. Otro régimen de dos gotas al día que proporcionaría tres medicamentos es la combinación de dosis fija de netarsudil / latanoprost (Rocklatan) que se aplica en la noche, con timolol aplicada en la mañana.
Cualquiera de estos regímenes le proporciona al paciente tres medicamentos con sólo dos gotas por día. La misma lógica se podría utilizar para proporcionar cuatro medicamentos con tres gotas al día, o cinco medicamentos con cuatro gotas al día. (Ver tabla 2) En resumen, la combinación de las drogas nos da mejores opciones para abordar la cuestión del cumplimiento del paciente.
Regímenes de tres a cinco medicamentos diarios para disminuir la PIO

Tabla 2. Regímenes de tres a cinco medicamentos diarios para disminuir la PIO.
Vale la pena preguntar si se puede esperar que nuestros pacientes administren de manera confiable tres o más gotas tópicas por día. De hecho, sabemos por nuestras propias prácticas, que muchos de nuestros pacientes llegan a utilizar tres o más gotas y están bien controlados. (Es cierto que el cumplimiento es difícil de medir, pero el sustituto del cumplimiento es nuestra medición de la PIO en el consultorio y la estabilidad de los campos visuales, el examen del nervio óptico y nuestras evaluaciones de la capa de fibra nerviosa). Por lo tanto, un régimen que consiste en múltiples gotas, puede funcionar para algunos pacientes. La cuestión es saber cuándo el dicho régimen no está funcionando.
¿Deberíamos ajustar la terapia?
Hay varias cosas que se deben considerar como señales de advertencia de que un régimen complejo no está funcionando para uno de nuestros pacientes:
El paciente dice, “Voy a mejorar. Verán, mi presión va a estar mejor la próxima vez”. Esta es una señal de alerta de que se necesita pensar en alternativas.
La presión varía mucho de visita a visita. La razón podría implicar el cumplimiento o que los medicamentos no funcionan; de cualquier manera, se debe pasar a otras opciones de tratamiento.
El paciente no ha pedido que se le renueve la receta en un año. Eso indica que, por alguna razón, el paciente no está usando o no está comprando, los medicamentos.
El paciente no acude a las citas programadas. Si el paciente no cumple con las visitas al consultorio, es probable que tampoco cumpla con los medicamentos.
También se debe estar atento a un problema cuando el paciente es de avanzada edad. Algunos pacientes de avanzada edad sufren de temblores o dificultad para exprimir un dispensador. En una situación así, se debe enfrentar una discusión honesta: ¿Hay alguien más en casa, o un cuidador, que pueda ayudar a instilar los medicamentos? Si no es así, entonces se tendrá que considerar otras opciones como la simplificación del régimen o elegir una opción quirúrgica o con láser.
Mi regla general es que, si el paciente no tiene quejas y está estable, es mejor dejar las cosas como estaban. Sin embargo, incluso si todo parece estar bien, hay dos opciones que se deberían considerar. En primer lugar, puede ser posible simplificar el régimen. Si se puede disminuir la cantidad de gotas que el paciente tiene que usar cambiando a una gota combinada, suponiendo que la cuestión de costos no sea un problema, entonces ofrezca esa opción al paciente.
En segundo lugar, si el paciente ha estado estable durante algún tiempo, podría valer la pena considerar la realización de un ensayo terapéutico inverso. Es posible que una de las gotas que esté usando el paciente ya no signifique una gran diferencia. Si este es el caso, estaría haciendo un favor al paciente al eliminarla.
Por ejemplo, si un paciente ha sido bien controlado en tres medicamentos durante varios meses o años, uno puede preguntarse si alguno podría ser eliminado. Si el paciente está interesado en simplificar el régimen, puede sugerir suspender un medicamento durante dos a cuatro semanas; luego, el paciente puede regresar para un chequeo para ver si todo está bien. (Si el paciente está descontento debido a un efecto secundario, esta también es una forma de determinar si ese medicamento es la causa).
El reto de invertir las pruebas terapéuticas es que los pacientes a menudo no quieren realizar las visitas adicionales al consultorio. Puede ser difícil convencer a un paciente que deje un medicamento y que regrese para el seguimiento si no está lo suficientemente preocupado por el régimen o por sus efectos secundarios. En ese caso, simplemente se debe mantener el rumbo.
No hay respuestas fáciles
¿Existe un régimen “mejor”? No. El máximo número de medicamentos que es efectivo, tolerado y que no menoscaba el cumplimiento, varía dramáticamente. Lo que pudiera ser un excelente tratamiento para un paciente puede ser intolerable para otro.
En este momento no tenemos una explicación clara, pero no hay duda de que existe una respuesta individual a la terapia médica, tal como también existe para la cirugía o cualquier otro tratamiento. Así que, para los médicos, encontrar el mejor régimen, es un proceso de ensayo y error. Lo que funciona mejor para un paciente dado, rara vez coincidirá con el resultado de un estudio clínico; el paciente siempre se encontrará en algún lugar de la curva. Nosotros como médicos, debemos estar sensibles a esta situación.
Quizás nuestro mayor desafío actual es que tenemos datos limitados sobre la eficacia de los nuevos medicamentos cuando se usan en combinación con otros medicamentos, y no sabemos si éstas combinaciones ayudarán o no a retrasar la cirugía. Sin embargo, tal y como se señaló anteriormente, sabemos que en muchas situaciones la adición de incluso una cuarta o quinta gota, proporcionará un descenso adicional de la presión. Y podemos suponer que, si conseguimos una reducción de la presión, eso retrasará cualquier posible intervención quirúrgica mientras los medicamentos sean efectivos y tolerados.
Como médicos, nuestro trabajo es asegurarnos que se logre la presión objetivo, que el glaucoma sea estable y que el paciente sea cumplido y adherente. Cualquiera que sea la cantidad de gotas que lo haga posible, esa es la cantidad correcta para ese paciente.
La Dra. Serle es profesora emérita de oftalmología en la Escuela de Medicina Icahn del Mount Sinai de Nueva York. Es consultora y accionista en Aerie Pharmaceuticals, un consultor de Allergan y Bausch + Lomb, y recibe subvenciones del Therapeutix ocular.
Referencias
Jampel HD, Chon BH, Stamper R, et al. Effectiveness of intraocular pressure-lowering medication determined by washout. JAMA Ophthalmol 2014;132:4:390-5.
Bro T, Lindén C. The more, the better? The usefulness of brimonidine as the fourth antiglaucoma eye drop. J Glaucoma 2018;27:7:643-646.
Spencer SKR, Shulruf B, McPherson ZE, et al. Factors affecting adherence to topical glaucoma therapy. Ophthalmol Glaucoma 2019;2:86-93.
Weinreb RN, Bacharach J, Fechtner RD, et al. 24-hour intraocular pressure control with fixed-dose combination brinzolamide 1%/brimonidine 0.2%: A multicenter, randomized trial. Ophthalmology 2019;126:8:1095-1104.
Banitt M, Jung H. Ocular surface disease in the glaucoma patient. Int Ophthalmol Clinics 2018;58:3:23-33.
de Fendi LI, Oliveira TC, et al. Additive effect of risk factors for trabeculectomy failure in glaucoma patients: A risk-group from a cohort study. J Glaucoma 2016;25:10;e879-883.
Ederer F, Gaasterland DE, Sullivan EK; AGIS Investigators. The Advanced Glaucoma Intervention Study (AGIS): 1. Study design and methods and baseline characteristics of study patients. Control Clin Trials 1994;15:4:299-325.
Gedde SJ, Schiffman JC, Feuer WJ, et al. Treatment outcomes in the Tube Versus Trabeculectomy (TVT) study after five years of follow-up. Am J Ophthalmol 2012;153:5:789-803.
Christakis PG, Tsai JC, Zurakowski D, Kalenak JW, et al. The Ahmed Versus Baerveldt study: Design, baseline patient characteristics, and intraoperative complications. Ophthalmology 2011;118:2172-9.
Inazaki H, Kobayashi S, Anzai Y, et al. One-year efficacy of adjunctive use of Ripasudil, a rho-kinase inhibitor, in patients with glaucoma inadequately controlled with maximum medical therapy. Graefes Arch Clin Exp Ophthalmol 2017;255:2009-15.
Weinreb R, Feldman RM, et al. MIGS: When maximum medical therapy is not enough. Eyenet Supplement 2018.
Serle JB, Goldberg JL, Herndon LW, et al. Changing the course of glaucoma: Clinical implications of new therapies for IOP control. Eyenet Supplement 2018.
Ustaoglu M, Shiuey E, Sanvicente C, et al. The efficacy and safety profile of Netarsudil 0.02% in glaucoma treatment: Real-world outcomes. Invest. Ophthalmol. Vis. Sci.. 2019; 60(9):2393.
Shin DH, McCracken MS, Bendel RE, et al. The additive effect of latanoprost to maximum-tolerated medications with low-dose, high-dose, or no pilocarpine therapy. Ophthalmology 1999;106:386-390.
Bayer A, Tas A, Sobaci G, Henderer JD. Efficacy of latanoprost additive therapy on uncontrolled glaucoma. Ophthalmologica 2002;216:443-8.
Feldman RM, Bell NP, Nagi KS. Control of intraocular pressure fluctuation: Are combination drugs more effective? Exp Review Ophthalmol 2011;6:2:151-4.
Kim JH, Caprioli J. Intraocular pressure fluctuation: Is it important? J Ophthalmic Vis Res 2018;13:170-4.
Lamberg H, Kumar N,Reed D, et al. Early clinical experience with latanoprostene bunod. IOVS 2019;60:2395.
Kahook MY, Serle JB, Mah FS, et al. Long-term safety and ocular hypotensive efficacy evaluation of netarsudil ophthalmic solution. Am J Ophthalmol 2019;200:130-137.
Radell JE, Serle JB. Netarsudil/latanoprost fixed dose combination for the treatment of open-angle glaucoma or ocular hypertension. Drugs of Today 2019;55:9:1-12.
Weinreb RN, Liebmann JM, Martin KR, et al. Latanoprostene bunod 0.024% in subjects with open-angle glaucoma or ocular hypertension, pooled phase 3 study findings. J Glaucoma 2018;27:1:7-15.

